首頁>>服務范圍>>生物潔凈室工程>>制藥工業潔凈廠房工程
原料藥潔凈廠房設計施工
醫藥潔凈室應以微粒和微生物為主要控制對象,同時尚應規定環境的溫度、濕度、壓差、照度、噪聲等參數
1 藥品生產工藝及產品對溫度和濕度有特殊要求時,應根據工藝及產品要求確定;
2 藥品生產工藝及產品對溫度和濕度無特殊要求時,空氣潔凈度A級、B級、C級的醫藥潔凈室溫度應為20℃~24℃,相對濕度應為45%~60%;空氣潔凈度D級的醫藥潔凈室溫度應為18℃~26℃,相對濕度應為45%~65%;
產品詳情
原料藥潔凈廠房要求:
非無菌原料藥精制、干燥、粉碎、包裝等生產操作的暴露環境應當按照D級潔凈區的要求設置。
工藝布局要防止人流、物流之間的混雜和交叉污染,并符合下列要求。
分別設置人員和物流進入生產區域的通道,必要時應設置極易造成污染的物料和廢棄物的專用出入口;
潔凈區內的半成品不宜直接進入一般生產區,可采用傳遞窗(柜)、氣閘或設置相應的設施進入一般生產區,傳輸帶不得穿越不同潔凈級別區域。
人員流動與凈化的原則是使發生交叉污染的可能性最小;適當情況下采用氣鎖;一般應具備雨具存放﹑脫外衣換鞋﹑洗手消毒﹑穿潔凈工衣﹑氣閘等功能。潔凈度按凈化程序,由外及里逐次提高。
氣鎖間兩側的門不應同時打開。可采用連鎖系統,或光學或(和)聲學的報警系統,或兩側相互可視,防止兩側的門同時打開;
潔凈廠房入口設雙面凈鞋設施(凳﹑臺﹑柜),供不同要求的鞋要能分開放置。洗手消毒間應設洗手盆﹑消毒和干手設施。
進入潔凈區域的原輔料﹑包裝材料,應有清潔措施。可設置原輔料外包清潔室﹑包裝材料清潔室﹑滅菌室等。
潔凈室或滅菌室之間應設置氣閘室或傳遞窗(柜);
生產過程中廢棄物出口不應與物料進口合用一個氣閘或傳遞窗(柜),宜單獨設置廢棄物傳遞裝置。
物料清潔室與潔凈室(區)之間應設置氣閘室或傳遞窗(柜),用于傳遞清潔或滅菌后的原輔料、包裝材料和其他物品。
傳遞窗(柜)兩邊的傳遞門,應有防止同時被打開的措施,密封性好并易于清潔。傳遞窗(柜)的尺寸和結構應滿足傳遞物品的大小和重量所需要求。
最終用于固體口服制劑的API 產品的操作區域(包括溶解、結晶、離心分離、干燥、混合、粉碎、包裝等)其環境空氣的潔凈度必須符合無菌產品的D級區標準。
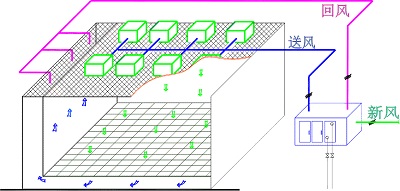
對于最終原料將成為無菌產品的生產區域而言,其環境的潔凈等級應達到無菌產品的C級標準。這通常要求為其提供高效過濾送風、低位回風、壓力氣鎖室(將暴露的粉體保持在潔凈室內)、以及為驗證房間潔凈條件所需的儀表。而最終藥品處理區的環境級別必須與這些API在其最終成品生產區的級別相一致。而對于最終生產無菌產品的API而言,其原料處理區的級別至少要滿足C 級或 D級的要求,并配備有空氣過濾、壓差控制和氣鎖等。
? 生產用潔凈室應配有低位或高/低位組合式回風。
? 在固體加料、料桶轉運、人孔和液體溢出等部位需設置局部排風系統LEV。
?由于中間品的生產都處于密閉狀態下,并且溫度受到控制,因此環境區域不需要控制。
? 一般而言,如沒有易燃溶媒的存在,那么HVAC系統可以再循環。
? AHU過濾應配備MERV 7和MERV 13。末端過濾器的等級評定應能適應產品要求。
? 強效API排風不得回流到潔凈室。建議為強效產品的排風采用洗氣塔或HEPA過濾器。
相關規范:
《藥品生產質量管理規范》2010
GB 5045750687-2019醫藥工業潔凈廠房設計標準
GB 50073-2013 潔凈廠房設計規范
GB 51110-2015 潔凈廠房施工及質量驗收規范
GB 50019-2015 工業建筑供暖通風與空氣調節設計規范
GB 50243-2016通風與空調工程施工質量驗收規范
GB 50016—2014(2018年版)建筑設計防火規范
上一篇:固體制劑凈化車間設計施工
下一篇:沒有了